Metano ch4 fotografías e imágenes de alta resolución Alamy
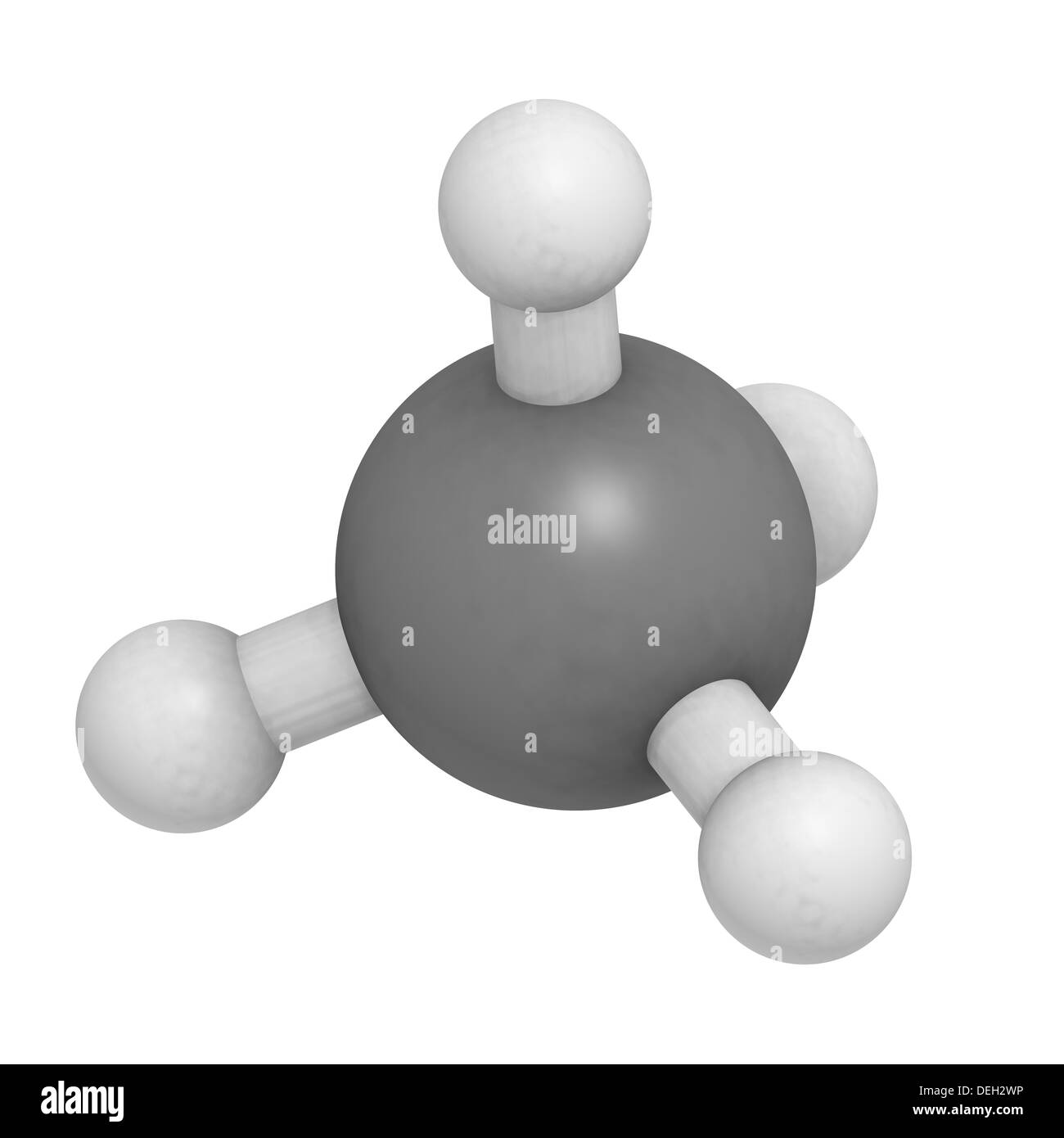
Tenemos que el compuesto CH₄ posee un enlace covalente. La razón de que ocurre un enlace covalente es que cada átomo de hidrógeno esta unido a un solo átomo de carbono, es decir, hay 4 átomos de hidrógeno unidos a un solo átomo de carbono. El CH₄ es la formula química del metano. Por lo general el enlace covalente se forma entre dos.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar
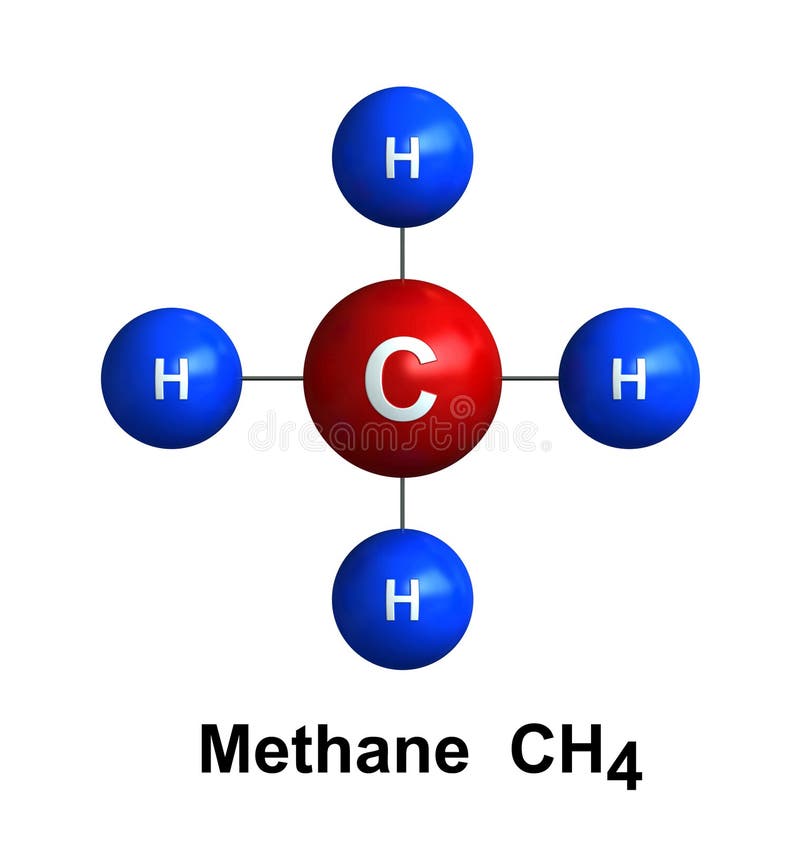
Un enlace químico es una atracción entre los átomos que permite la formación de sustancias químicas que contienen dos o más átomos. La unión es causada por la fuerza electrostática de atracción entre cargas opuestas, ya sea entre electrones y núcleos, o como resultado de una atracción dipolo. Todos los enlaces se pueden explicar.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar
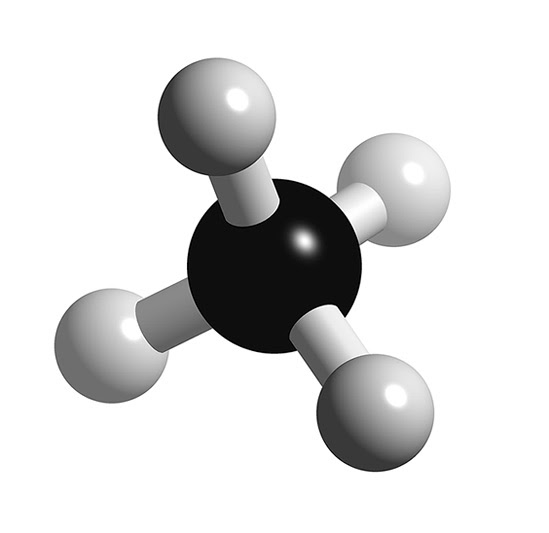
Predicción del tipo de enlace (electronegatividad) Reportar un problema. Haz 4 problemas. Aprende gratuitamente sobre matemáticas, arte, programación, economía, física, química, biología, medicina, finanzas, historia y más. Khan Academy es una organización sin fines de lucro, con la misión de proveer una educación gratuita de clase.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar

El metano es considerado un hidrocarburo alcano de los más simples que existen. Su fórmula química es CH4. Es decir que está formado por un átomo de carbono y cuatro átomos de hidrógeno. Están unidos por enlaces covalentes. El metano es un gas muy inflamable y que es poco soluble en agua. Es uno de los compuestos responsable del efecto.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar

#MetanoEnlaceCovalente#EnlaceCovalenteMetano#EnlaceCovalenteCH4SUSCRIBETE http://www.youtube.com/c/PROFEARANTXA?sub_confirmation=1, si el video te ha servido.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar 09/2023

El metano, (\(\ce{CH4}\), es un solo átomo de carbono unido covalentemente a cuatro átomos de hidrógeno. En estos ejemplos los átomos centrales forman diferentes números de enlaces a los átomos de hidrógeno para completar su subcapa de valencia y formar octetos. Figura \(\PageIndex{4}\): Ejemplos de moléculas 3D. De izquierda a derecha.
Átomos y Moléculas, Sustancias Orgánicas
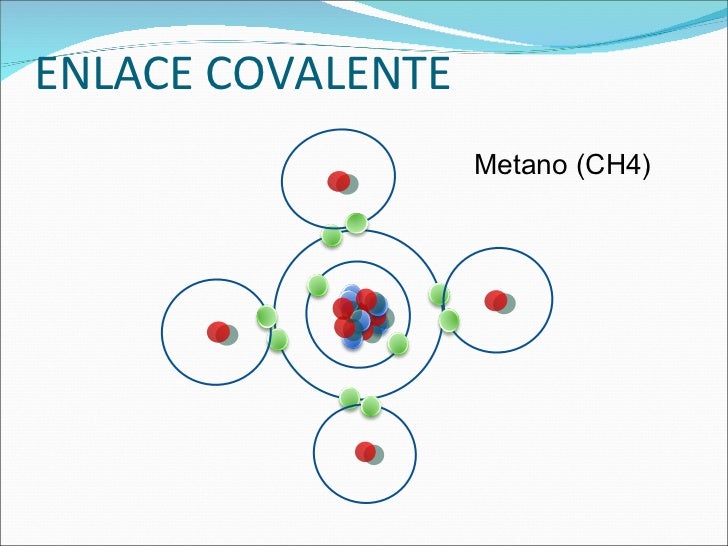
El CH4, también conocido como metano, es una molécula formada por un átomo de carbono enlazado a cuatro átomos de hidrógeno. Estos enlaces son de tipo covalente, lo que significa que los átomos comparten pares de electrones para formar la molécula. Cada átomo de hidrógeno forma un enlace covalente con el átomo de carbono, resultando.
Metano ch4 Imágenes recortadas de stock Alamy
El metano (del griego methy vino, y el sufijo -ano) [2] es el hidrocarburo alcano más sencillo, cuya fórmula química es C H 4. [3] Cada uno de los átomos de hidrógeno está unido al carbono por medio de un enlace covalente.Es una sustancia no polar que se presenta en forma de gas a temperaturas y presiones ordinarias. Es incoloro, inodoro e insoluble en agua.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar 09/2023
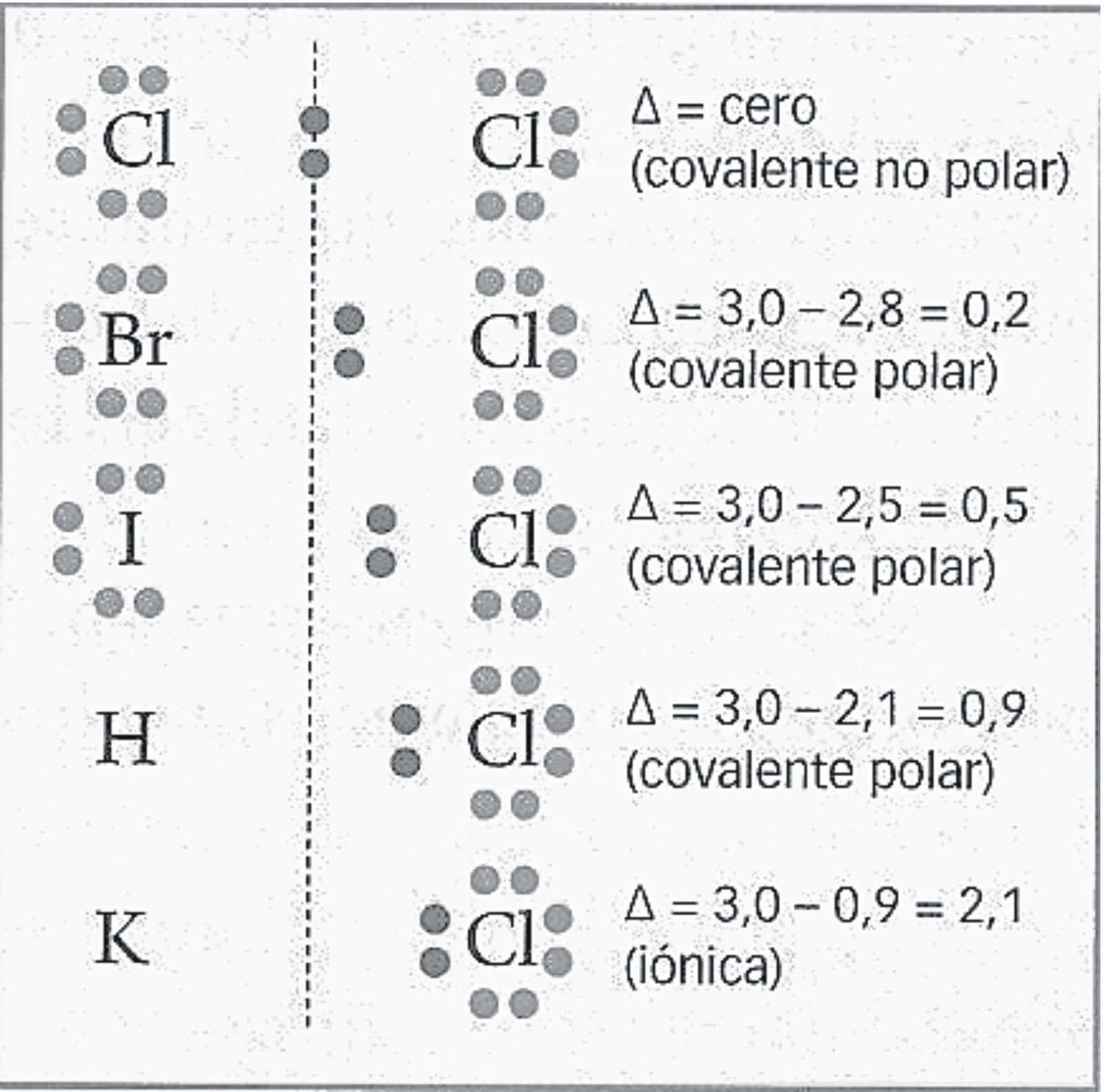
Puro vs. enlaces covalentes polares. Si los átomos que forman un enlace covalente son idénticos, como en H 2, Cl 2, y otras moléculas diatómicas, entonces los electrones en el enlace deben ser compartidos por igual.Nos referimos a esto como un enlace covalente puro.Los electrones compartidos en enlaces covalentes puros tienen la misma probabilidad de estar cerca de cada núcleo.
Modelo molecular de la molécula de metano (CH4). Ilustración de vectores Imagen Vector de stock
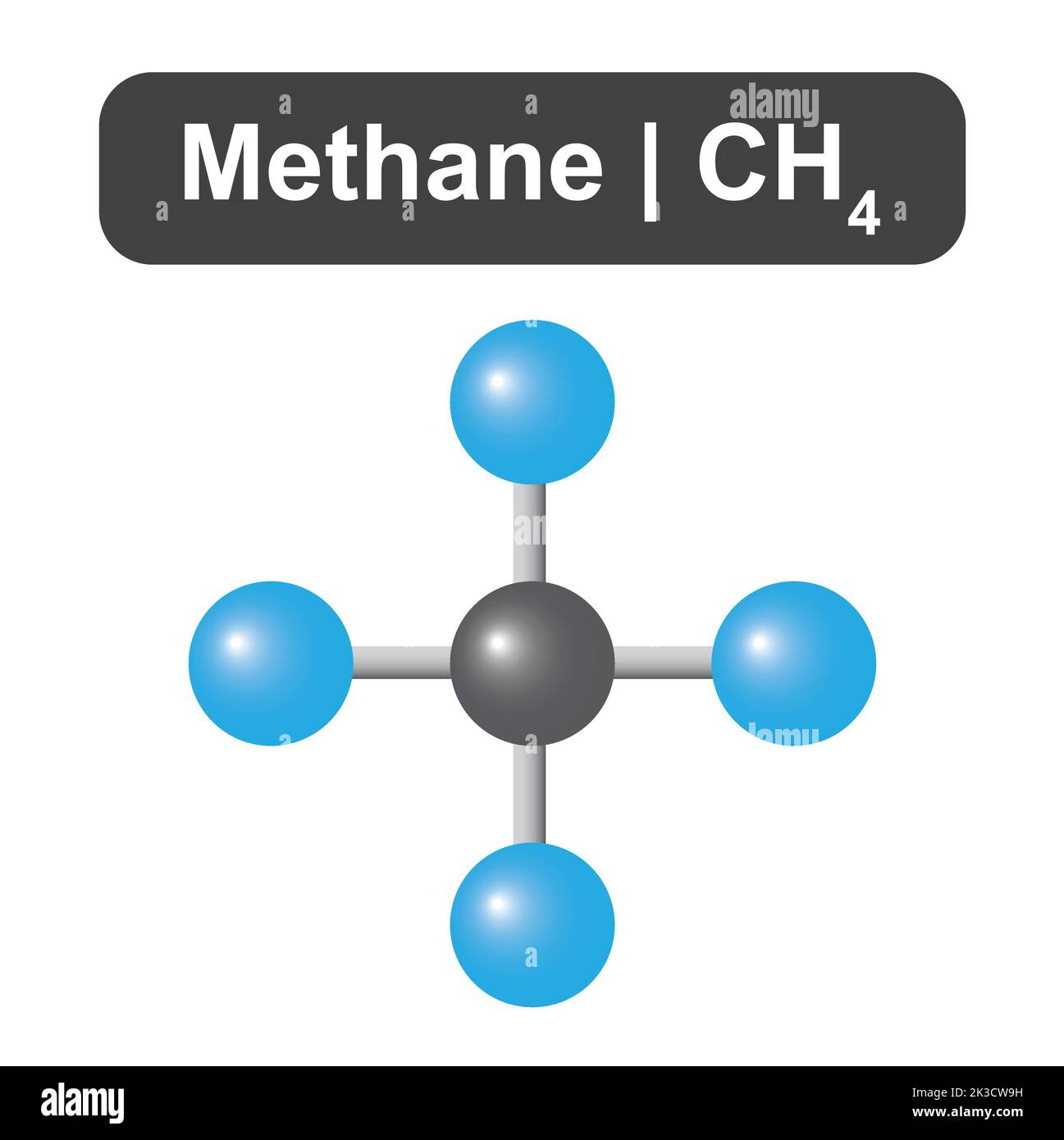
En la estructura de Lewis del CH4 se dibuja un átomo de carbono conectado por cuatro enlaces covalentes a cuatro átomos de hidrógeno. Cada línea representa un par de electrones compartidos que forman los enlaces. Esta representación ayuda a visualizar la disposición de los átomos y los electrones en la molécula de metano.
Fórmula química del metano. Modelo 3D de la molécula de CH4. Ilustración vectorial Imagen Vector

El CH4, también conocido como metano, es un gas incoloro e inodoro que se encuentra de forma natural en el ambiente. Este compuesto está compuesto por un átomo de carbono y cuatro átomos de hidrógeno, y su estructura molecular se forma a través de un tipo de enlace llamado "enlace covalente". En este artículo, exploraremos en más.
PPT ENLACE QUÍMICO PowerPoint Presentation, free download ID844764

El enlace dativo es un tipo especial de enlace simple que consiste en que el par de electrones proviene solo de uno de los dos átomos enlazados. Es decir, pudiera verse como una "compartición forzada". Por ejemplo, la molécula H 2 O utiliza uno de los pares libres de oxígeno para donárselos a un ion H + (H 2 O: → H + = [H 2 O-H] + o.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar
Enlaces químicos. Los enlaces químicos mantienen unidas a las moléculas y crean conexiones temporales que son esenciales para la vida. Los tipos de enlace químico que se incluyen son covalente, iónico, así como enlaces de hidrógeno y fuerzas de dispersión de London.
Arriba 97+ Foto Tipo De Enlace Que Presenta El Compuesto Ch4 Actualizar 09/2023
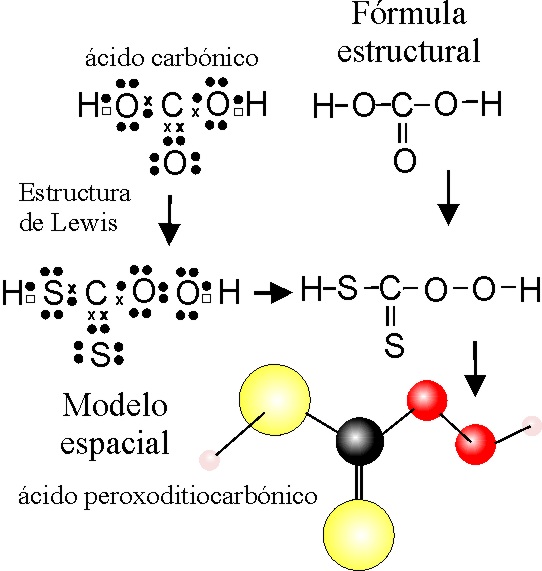
Formulación y nomenclatura de CH4, tetrahidruro de carbono, metano | formulacionquimica.com.. Tipo de compuesto: alcano. C. Carbono-2, +2, +4. No metal. H. Hidrógeno +1.. Cada uno de los átomos de hidrógeno se encuentra unido a al carbono mediante un enlace covalente. El metano es el componente fundamental del gas natural.
Covalent Bond — Formation & Compounds Expii

Enlaces polares pero globalmente apolar. La molécula de metano, CH4, debido a su geometría tetraédrica, es apolar a pesar de presentar enlaces C-H polares (porque el carbono y el hidrógeno tienen distinta electronegatividad). Esto se debe a que la geometría hace que los momentos dipolares individuales de cada uno de los enlaces se anulen.
CH4 Lewis Structure How to Draw the Dot Structure for CH4 (Methane) YouTube
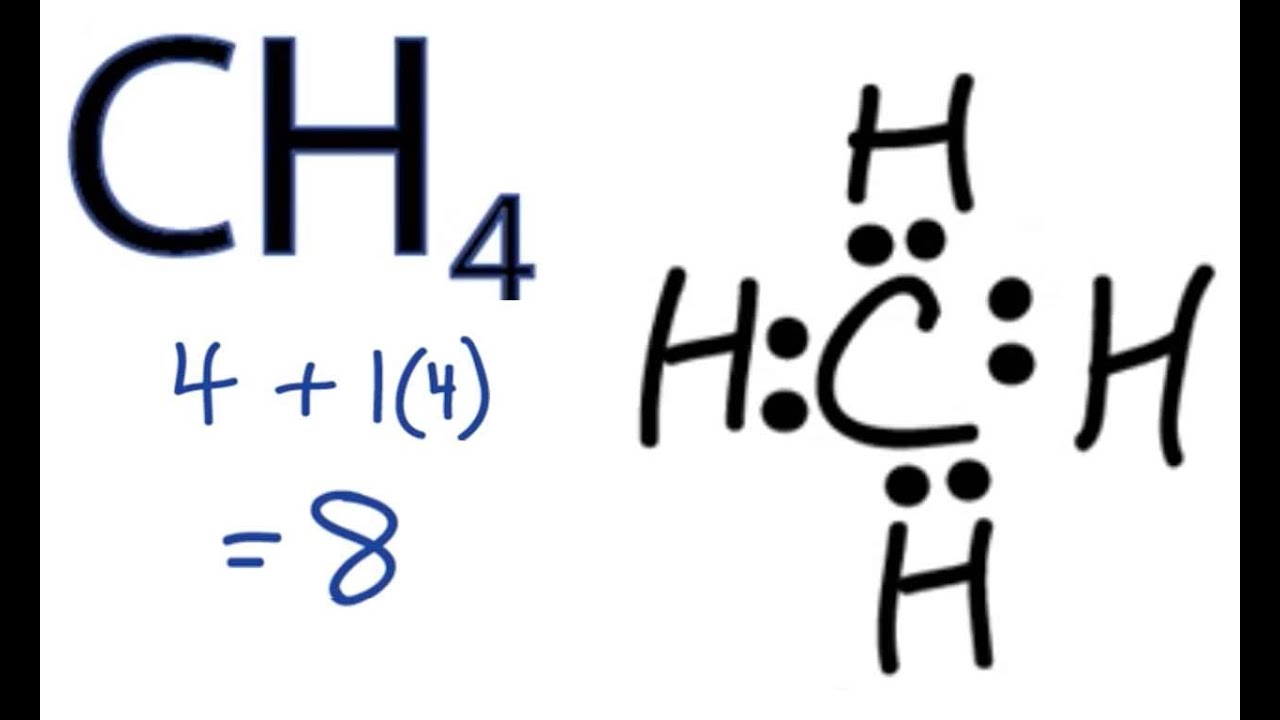
En el caso del H 2, el enlace covalente es muy fuerte; hay que añadir una gran cantidad de energía, 436 kJ, para romper los enlaces en un mol de moléculas de hidrógeno y hacer que los átomos se separen: H2(g) 2H(g) ΔH = 436kJ H 2 ( g) 2 H ( g) Δ H = 436 kJ. De manera inversa, se libera la misma cantidad de energía cuando se forma un mol.
.